corrigé exos chimie absorbance
Publié le 11/04/2026
Extrait du document
«
Exercice 31 p.54
Enoncé : Un éthylotest contient des ions dichromate Cr2O72−(aq) jaunes qui oxydent
l'éthanol C2H6O(aq) expiré par le conducteur pour former des ions chrome Cr3+(aq) verts et
de l'acide éthanoïque C2H4O2(aq)
Données: couples d'oxydoréduction : Cr2O72−(aq)/Cr3+(aq) et C2H4O2(aq)/C2H6O(aq)
1.
Écrire l'équation de la réaction d'oxydation de l'éthanol par les ions dichromate.
C2H6O(aq) + H20(l) = C2H4O2(aq) + 4 H+(aq) + 4 e(*3)
2+
3+
Cr2O7 (aq) + 14H (aq) + 6e = 2 Cr (aq) + 7 H20(l)
(*2)
3 C2H6O(aq) + 2 Cr2O72-(aq) + 16 H+(aq) ⇌ 4Cr3+(aq) + 11 H20(l) + 3 C2H4O2(aq)
2.
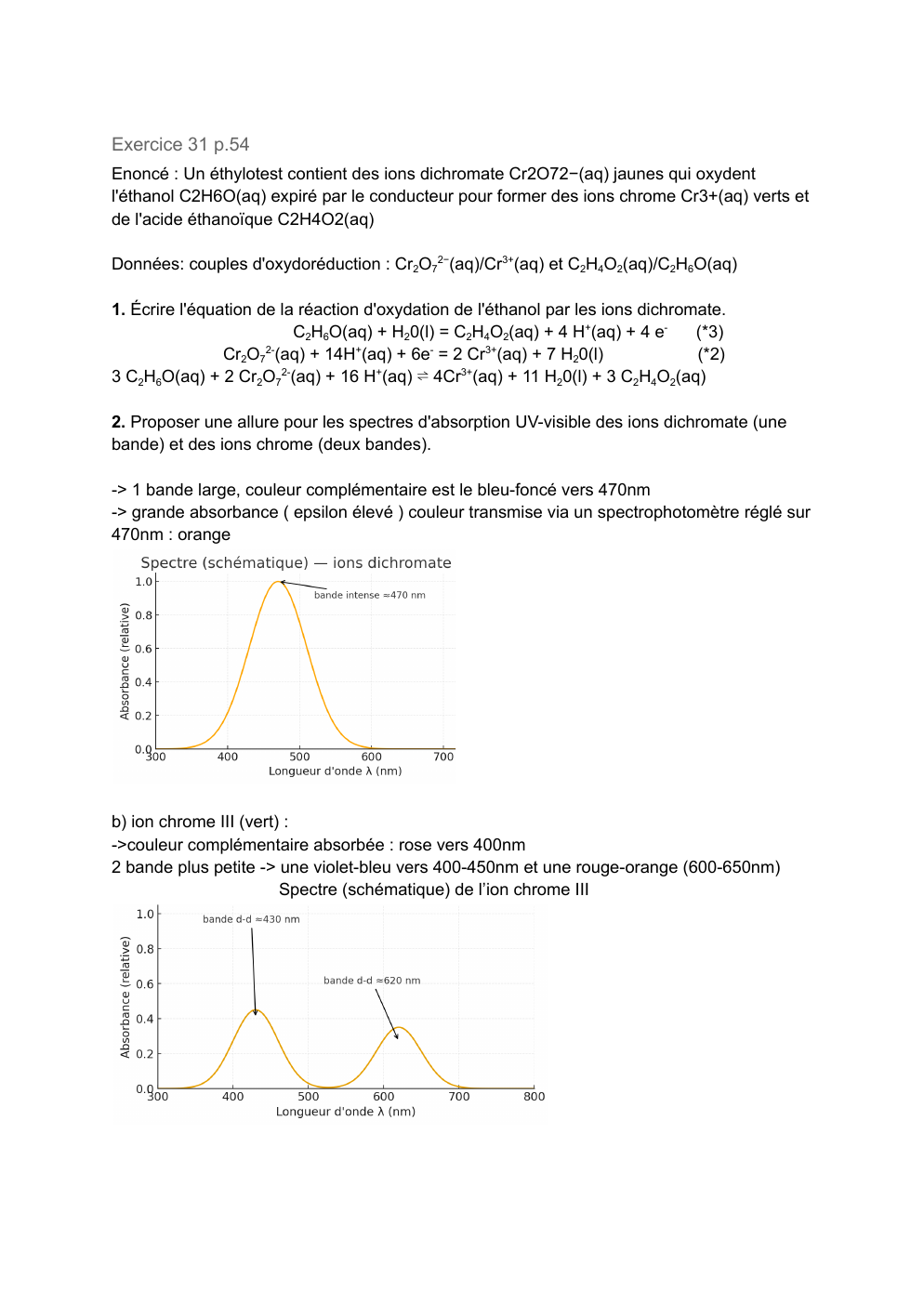
Proposer une allure pour les spectres d'absorption UV-visible des ions dichromate (une
bande) et des ions chrome (deux bandes).
-> 1 bande large, couleur complémentaire est le bleu-foncé vers 470nm
-> grande absorbance ( epsilon élevé ) couleur transmise via un spectrophotomètre réglé sur
470nm : orange
b) ion chrome III (vert) :
->couleur complémentaire absorbée : rose vers 400nm
2 bande plus petite -> une violet-bleu vers 400-450nm et une rouge-orange (600-650nm)
Spectre (schématique) de l’ion chrome III
3.
Préciser quelles sont les principales bandes caractéristiques présentes sur le spectre IR
de l'éthanol ainsi que sur celui de l'acide éthanoïque
Ethanol : liaison O-H (3000-3500 cm-1) bande large-moyenne et C-H ( 2850-3100 cm-1)
Acide éthanoïque : O-H ( bande large 2500-3200)
liaison C double liaison O (1680-1710 carboxyle)
Exercice 37 p.57
1. On remarque deux pics d'absorption sur le spectre, le plus important se situe aux
alentours de λ≃400nm.
D’après le cercle chromatique, cette longueur d’onde
correspond au violet, or la couleur complémentaire au violet est le vert.
Le deuxième
pic, moins important, se trouve vers λ≃700nm, soit du rouge, dont la couleur
complémentaire est le bleu-vert.
La solution apparaît donc verte, légèrement bleutée.
2. σ = λNi2+ x [Ni2+(aq)] + λCl- x [Cl-(aq)]
σ = λNi2+ x c1 + λCl- x 2c1 = c1 (λNi2+ + 2λCl- )
⇔c1 = σ / (λNi2+ + 2λCl- )
avec σ=7,556 mS.cm-1=7,556 x 102 mS.m-1
λNi2+=9,9 mS.m2.mol-1 ; λCl-=7,6 mS.m2.mol-1
c1 = 7,556 x102 / (9,9 + 2 x 7,6) = 30 mol.m-3 = 3,0 x 10-2 mol.L-1
3. A720nm = ε x ℓ x c1’
⇔c1’ = A720nm / ( ε x ℓ )
avec A=0,663 ; ε=22,1 L.mol-1.cm-1 ; ℓ=1,0cm
c1’ = 0,663 / (22,1 x 1,0....
»
↓↓↓ APERÇU DU DOCUMENT ↓↓↓
Liens utiles
- Corrigé physique chimie 1ère transformation
- Grand Oral de Physique-Chimie : Améliorer les Imageries par Résonance Magnétique (IRM)
- bac physique: CHAPITRE 01 : NOMENCLATURE EN CHIMIE ORGANIQUE
- Physique chimie - année 2000
- Grand oral chimie: : Dans quelles mesures la radioactivité est-elle utilisée en médecine nucléaire ?